Projekt J3-4516
Vloga neoantigenov pri nedrobnoceličnem raku pljuč
Raziskovalni projekt ARIS
Evidenčna številka: J3-4516
Obdobje 1.10.2022 - 30.9.2025
Vodja: asist. dr. Julij Šelb, dr. med., spec.
Raziskovalna dejavnost: Medicina/Reprodukcija človeka
Seznam sodelujočih raziskovalnih organizacij: Univerzitetna klinika za pljučne bolezni in alergijo Golnik; Nacionalni inštitut za biologijo
Vsebinski opis projekta
Učinkovito protitumorsko imunost pri ljudeh je v veliki meri mogoče pripisati T-celicam, usmerjenim proti neoantigenom, ki so prisotni na tumorskih celicah. Neoantigeni so skupina proteinov, ki so vezani na HLA molekule in nastanejo zaradi tumorsko specifičnih mutacij. Ker zaobidejo centralno timično toleranco imajo visok imunogeni potencial . Zato predstavljajo dobro tarčo za protitumorsko imunost.
Pljučni rak je med najpogostejšimi in daleč najbolj smrtonosnimi vrstami raka. Ker je kajenje glavni dejavnik tveganja za razvoj pljučnega raka, je skupaj z drugimi vrstami raka, ki so izpostavljeni veliki obremenitvi s kancerogeni, tudi med najbolj s somatskimi mutacijami (in verjetno tudi neoantigeni) obremenjenimi tipi rakov.
Koncept neoantigenov se uspešno uporablja pri rutinski obravnavi pljučnega in drugih rakov, predvsem pri zdravljenju teh bolnikov z zaviralci kontrolnih točk imunskega odziva (ZKTIO). Nedavno je FDA odobrila zdravljenje z ZKTIO pembrolizumabom pri posameznikih z napredovalimi tumorji, ki imajo visoko tumorsko mutacijsko breme (TMB; ≥10 mutacij/megabazo). TMB predstavlja posredno metodo ocene neoantigenskega bremena, vendar je veliko manj specifična, saj ocena TMB ne upošteva vseh bioloških korakov, potrebnih za predstavitev mutiranega zaporedja DNK kot neoantigena imunskemu sistemu.
ZKTIO delujejo samo na podskupino bolnikov; v splošni kohorti bolnikov z nedrobnoceličnim pljučnim rakom (NDRP) se le približno 20 % posameznikov odzove na zdravljenje. Ker imajo ZKTIO veliko neželenih učinkov (po nekaterih ocenah ima do 60 % bolnikov na ZKTIO neželene učinke) in so tudi draga zdravila, je zato izrednega pomena, da zdravljenje prejmejo le tisti, ki se bodo na zdravljenje odzvali. Vendar pa nimamo učinkovitih biomarkerjev, ki bi napovedali odziv na zdravljenje. Do danes sta bila samo zgoraj omenjeno TMB in imunohistokemična (IHK) ekspresija PD-L1 v tumorskem tkivu odobrena kot klinična označevalca za vodenje terapije z ZKTIO.
Različni multiparametrični modeli napovedi (ki upoštevajo več spremenljivk tako tumorja kot gostitelja) redno kažejo izboljšano napovedovanje odziva na zdravljenje z ZKTIO v primerjavi s samo-TMB/samo-PD-L1 IHK. Dosledno je bil v teh modelih najpomembnejši napovedi dejavnik TMB. V skladu z biološkim sklepanjem je nedavna študija pokazala, da je obremenitev z neoantigeni (mutacije, ki se predstavijo in jih prepozna imunski sistem) boljši napovedni dejavnik odziva na zdravljenje z ZKTIO kot TMB. Domnevamo, da bo uporaba neoantigenske obremenitve v takem kontekstu bistveno izboljšala natančnost napovedi takšnega modela; to bo tudi osrednja hipoteza sedanjega projekta.
Zato v projektu načrtujemo vzpostavitev algoritmov za napovedovanje neoantigenov, vi-vitro validacijo rezultatov teh algoritmov in uporabo teh rezultatov (t.i. obremenitev z neoantigeni) za izboljšanje modelov napovedovanja odziva na zdravljenje z ZKTIO. Poleg tega bomo ocenili umestitev celotnega koncepta uporabe z neoantigeni izboljšanega postopka napovedovanja odziva na zdravljenje z ZKTIO v lokalno rutinsko klinično prakso, da bi ugotovili, ali imajo lahko bolniki in lokalni zdravstveni sistem koristi od tega.
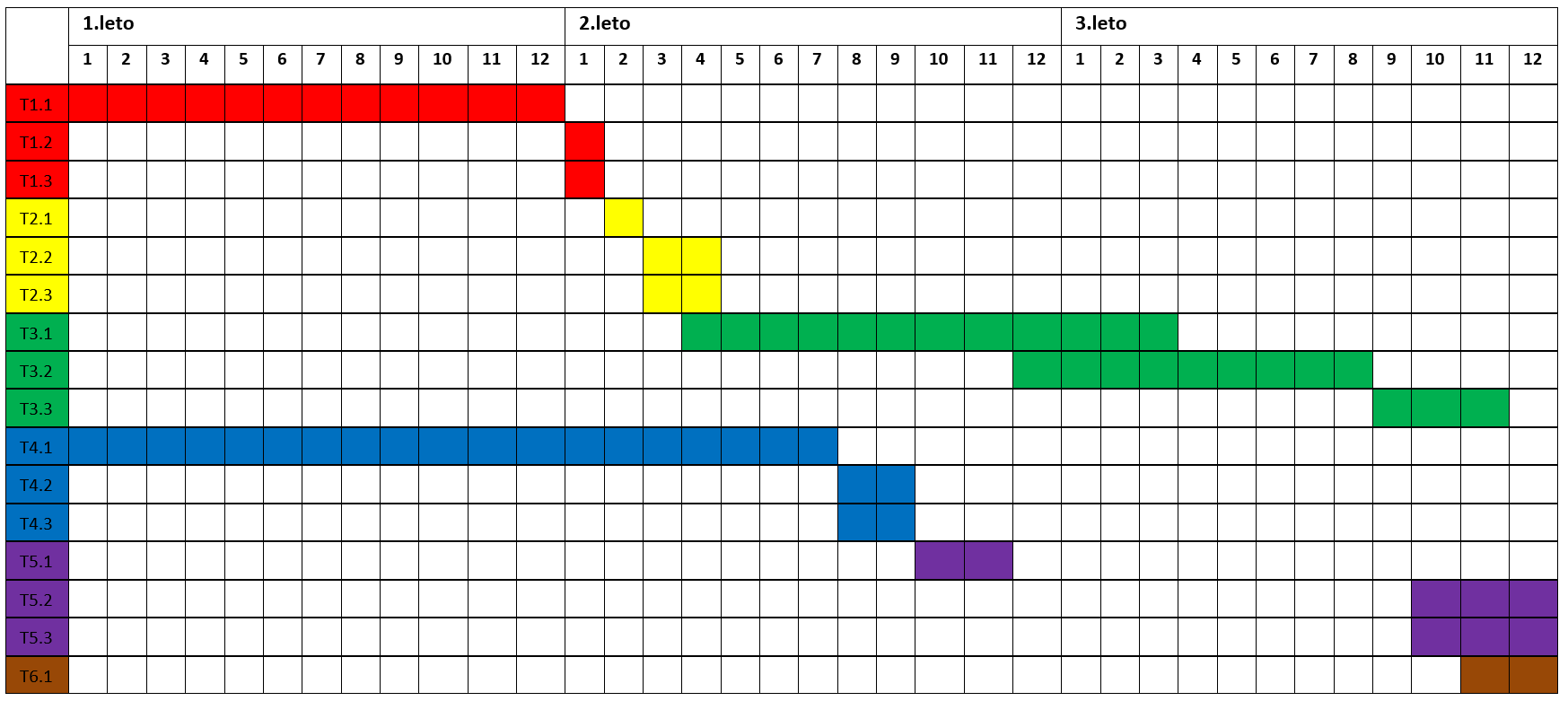
Časovnica projekta
|
Delovni paket (WP) |
Naloge (T) |
Mejniki in rezultati |
Porazdelitev dela |
|
WP1 Vzorčenje in sekvenciranje (DNK, RNA) |
T1.1 Vzorčenje bolnikov |
50 primernih bolnikov (napredni NDRP, 2 vzorca na tumor – centralna masa in tumorska bezgavka) pred začetkom zdravljenja z ZKTIO |
GUC |
|
T1.2 WES tumorjev |
Opravljenih bo 100 WES tumorjev (2 na pacienta) |
GUC |
|
|
T1.3 RNA sekvenciranje tumorskih vzorcev (centralna tumorska masa) |
Izvedenih bo 50 sekvenciranj RNA tumorskega vzorca (centralna tumorska masa). |
GUC |
|
|
WP2 Vzpostavitev uveljavljenih algoritmov za napovedovanje obremenitve z neoantigeni/ odziva na zdravljenje z ZKTIO |
T2.1 Postavitev algoritma za klicanje somatskih mutacij |
Algoritem za klicanje somatskih mutacij bo vzpostavljen in delujoč na strežnikih GUC |
GUC |
|
T2.2 Postavitev algoritmov za ugotavljanje bremena neoantigenov |
Algoritmi za ocenjevanje bremena neoantigenov bodo vzpostavljeni in delujoči na strežnikih GUC |
GUC |
|
|
T2.3 Postavitev algoritmov za napovedovanje odziva na zdravljenje z ZKTIO |
Algoritmi za napovedovanje odziva na zdravljenje z ZKTIO bodo vzpostavljeni in delujoči na strežnikih GUC |
GUC |
|
|
WP3 Eksperimentalna validacija prednostnih neoantigenskih kandidatov |
T3.1 Sinteza prednostnih neoantigenskih peptidov |
Predvideni 'predstavljeni in prepoznani' peptidi (neoantigeni) posameznikov z alelom HLA-A*02:01 bodo proizvedeni kot nona/dekamerji |
ICI-NIB |
|
T3.2 Izolacija/obogatitev CD8+ T celic iz periferne krvi |
Proizvodnja obogatenih neoantigen reaktivnih CD8+ T celic |
ICI-NIB |
|
|
T3.3 Vrednotenje reaktivnosti proti neoantigenom |
Izračunana bo sestavljena ocena reaktivnosti za vsak ocenjen neoantigenski peptid |
ICI-NIB |
|
|
WP4 Vrednotenje uveljavljenih algoritmov za napovedovanje odziva na zdravljenje z ZKTIO na trenutni kohorti |
T4.1 Zdravljenje bolnikov z ZKTIO |
Obravnava bolnikov v skladu z dobro klinično prakso |
GUC |
|
T4.2 Definiranje odzivnikov/neodzivnikov |
Bolniki bodo po 6 mesecih zdravljenja razvrščeni kot odzivni/neodzivni v skladu z RECIST |
GUC |
|
|
T4.3 Ocena uveljavljenih algoritmov za napovedovanje odziva na zdravljenje z ZKTIO |
Izdelan bo ROC-AUC za razlikovanje med odzivnimi/neodzivnimi bolniki glede na uveljavljene algoritme za napovedovanje odziva na zdravljenje z ZKTIO |
GUC |
|
|
WP5 Izpopolnitev modelov napovedi odziva na zdravljenje z ZKTIO z uporabo kohortnih podatkov projekta |
T5.1 Treniranje obstoječih algoritmov na kohortnih podatkih projekta |
Modeli, ki uporabljajo obstoječe napovedne dejavnike, bodo prilagojeni podatkom kohorte projekta |
GUC |
|
T5.2 Izpopolnitev obstoječih modelov z dodatnimi biološko verjetnimi napovednimi dejavniki |
Izpopolnjen model napovedi odziva na zdravljenje z ZKTIO bo treniran na kohortnih podatkih projekta |
GUC |
|
|
T5.3 Primerjava modelov med seboj |
Izdelan bo seznam modelov napovedi odziva na zdravljenje z ZKTIO, ki bodo razvrščeni glede na vrednosti ROC-AUC |
GUC |
|
|
WP6 Farmakoekonomska ocena uporabe najboljšega modela napovedi odziva na zdravljenje z ZKTIO v rutinski praksi v lokalnem okolju |
T6.1 Farmakoekonomska ocena uporabe najboljšega modela napovedi odziva na zdravljenje z ZKTIO v rutinski praksi v lokalnem okolju |
Izdelana bo farmakoekonomska ocena vključitve najboljšega modela za napovedovanje odziva na zdravljenje z ZKTIO v lokalno rutinsko klinično prakso |
GUC |
*GUC – Golnik university clinic; ICI-NIB - Immunology and Cellular Immunotherapy group na National Institute of Biology
Faze projekta in njihova realizacija


 04 25 69 700
04 25 69 700